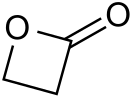
Пропиолактон
| Пропиолактон | |||
|---|---|---|---|
| |||
| Общие | |||
| Традиционные названия | β-пропиолактон | ||
| Хим. формула | C3H4O2 | ||
| Физические свойства | |||
| Молярная масса | 72,06 г/моль | ||
| Плотность | 1,146 г/см³ | ||
| Энергия ионизации | 9,7 эВ[2] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | −33,4 °C | ||
| • кипения | 162 °C | ||
| • разложения | 323 ± 1 ℉[1] | ||
| • вспышки | 165 ± 1 ℉[1] | ||
| Пределы взрываемости | 2,9 ± 0 об.%[1] | ||
| Давление пара | 3 ± 1 мм рт.ст.[1] | ||
| Структура | |||
| Дипольный момент | 1,4E−29 Кл·м[2] | ||
| Классификация | |||
| Рег. номер CAS | 57-57-8 | ||
| PubChem | 2365 | ||
| Рег. номер EINECS | 200-340-1 | ||
| SMILES | |||
| InChI | |||
| RTECS | RQ7350000 | ||
| ChEBI | 49073 | ||
| ChemSpider | 2275 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Пропиолактон, β-пропиолактон (оксетан-2-он) — бесцветная жидкость с резким запахом, внутренний циклический эфир β-оксипропионовой кислоты. Токсичен.
Реакционная способность[править | править код]
В силу напряжённости четырёхчленного цикла пропиолактон - высокореакционное соединение, для которого характерны реакции с раскрытием цикла.
При нагреве пропиолактон полимеризуется с образованием линейных полиэфиров [—ОСН2СН2С(О)—]n, такая же полимеризация может быть проведена в мягких условиях под действием различных катализаторов.
Пиролиз пропиолактона в газовой фазе ведёт к образованию этилена и диоксида углерода.
Будучи циклическим сложным эфиром, пропиолактон является электрофилом, направление нуклеофильной атаки зависит от природы нуклеофила: жёсткие нуклеофилы атакуют пропиолактон по карбонильному атому углерода, мягкие — по оксиметиленовому углероду:
Пропиолактон гидролизуется с образованием β-гидроксипропионовой кислоты, в нейтральных условиях и при кислотном катализе взаимодействие пропиолактона со спиртами и фенолом и ведет к образованию простых эфиров β-гидроксипропионовой кислоты, реакция с тиофенолом в этих условиях протекает аналогично:
- (CH2CH2O)CO + RXH RX(CH2)2COOH
- X = O, S
Взаимодействие аминов с пропиолактоном в ацетонитриле приводит к образованию как производных β-аминопропионовой кислоты (с аммиаком, этиламином, анилином):
- (CH2CH2O)CO + R1R2NH R1R2NH(CH2)2COOH ,
так и амидов β-гидроксипропионовой кислоты:
- (CH2CH2O)CO + R1R2NH HO(CH2)2CONR1R2
Получение[править | править код]
Получают пропиолактон каталитическим взаимодействием формальдегида (CH2O) с кетеном (CH2=С=О).
Применение[править | править код]
Растворы и пары пропиолактона обладают сильным бактерицидным действием; применяют его в медицине для стерилизации крови, вакцин, ферментов и др. биологических препаратов, а также как фумигант.
См. также[править | править код]
Примечания[править | править код]
- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0528.html
- ↑ 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
Это заготовка статьи об органическом веществе. Помогите Википедии, дополнив её. |
Для улучшения этой статьи желательно:
|